4-NITROPHENYL-ALPHA-D-MANOPYRANOSIDE CAS:10357-27-4 sivobel prašek 98%
| Kataloška številka | XD90011 |
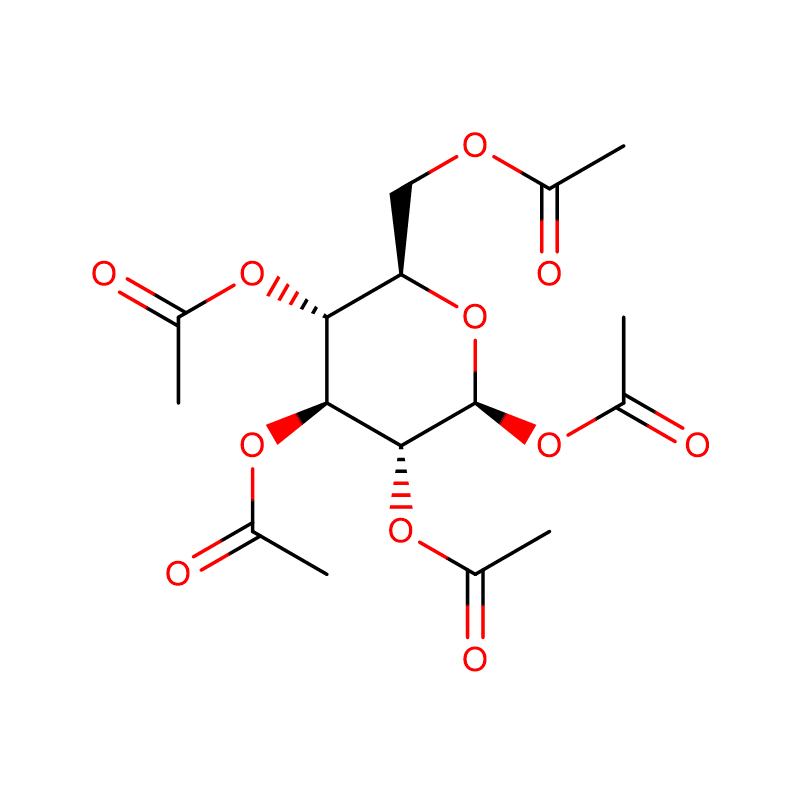
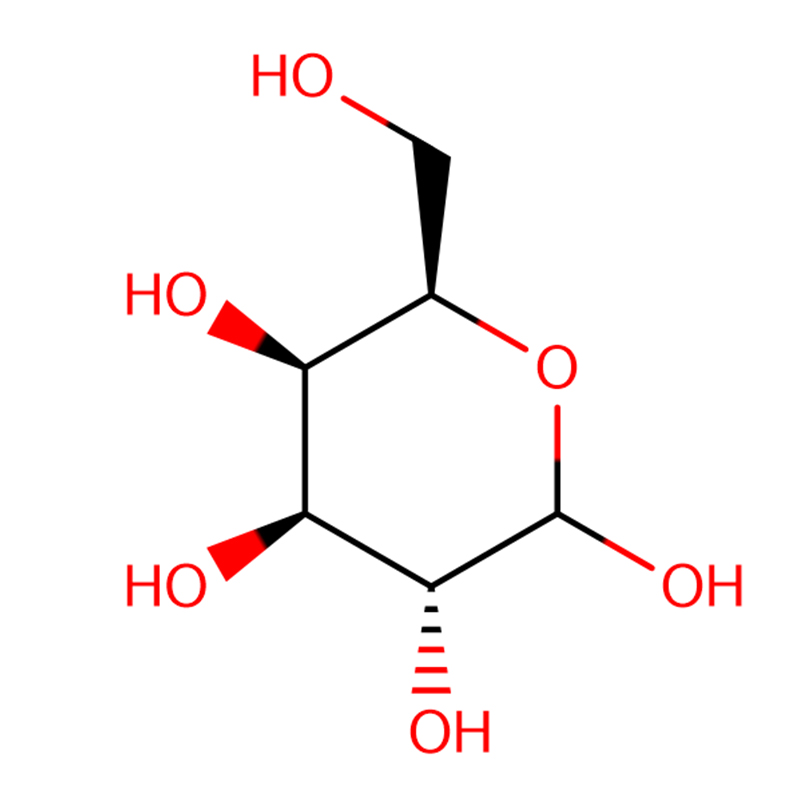
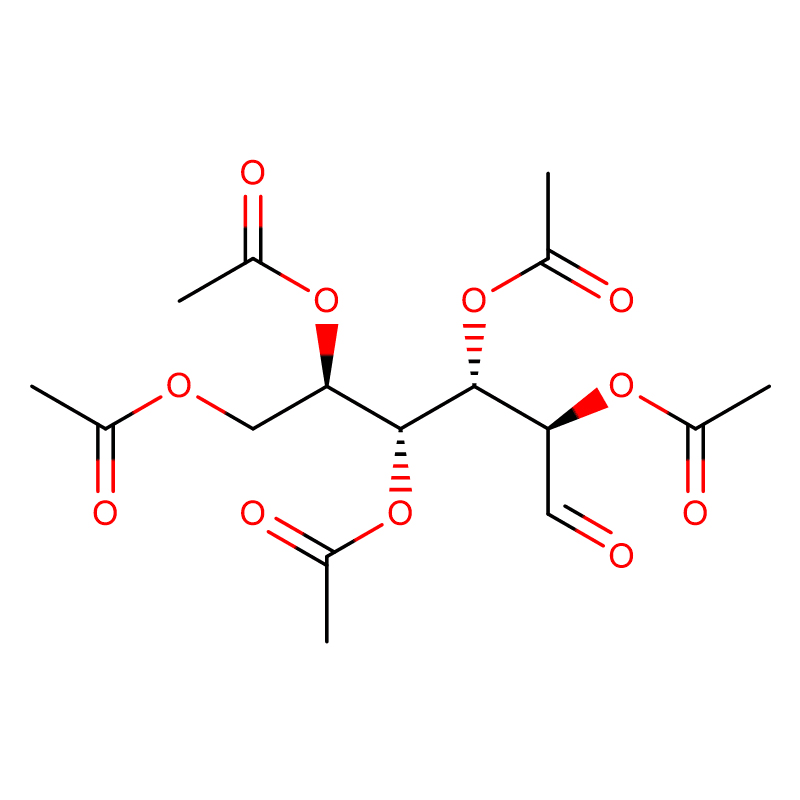
| ime izdelka | 4-nitrofenil-alfa-D-manopiranozid |
| CAS | 10357-27-4 |
| Molekularna formula | C12H15NO8 |
| Molekularna teža | 30301.25 |
| Podrobnosti o shranjevanju | -2do -8°C |
| Usklajena tarifna oznaka | 29400000 |
Specifikacije produkta
| voda | <5% Karl Fische |
| Topnost | 1 % v DMF je bister in brezbarven |
| Čistost | Prosti 4-nitrofenol <200 ppm |
| HPLC | > 98 % |
| Videz | Umazano bel prah |
Mehanski vpogled v družino alfa-manozidaz, ki je odvisna od Ca2+, v simbiontu človeškega črevesja.
Bakterije debelega črevesa, ki jih ponazarja Bacteroides thetaiotaomicron, igrajo ključno vlogo pri ohranjanju zdravja ljudi z izkoriščanjem velikih družin glikozidnih hidrolaz (GH) za izkoriščanje prehranskih polisaharidov in gostiteljskih glikanov kot hranil.Takšno širjenje družine GH ponazarja 23 glikozidaz družine GH92, kodiranih z genomom B. thetaiotaomicron.Tukaj pokažemo, da so to alfa-manozidaze, ki delujejo prek enega samega mehanizma izpodrivanja za uporabo gostiteljskih N-glikanov.Tridimenzionalna struktura dveh manozidaz GH92 opredeljuje družino dvodomenskih proteinov, v katerih se katalitično središče nahaja na vmesniku domene, ki zagotavlja pomoč kisline (glutamat) in baze (aspartat) pri hidrolizi v Ca(2+)- odvisen način.Tridimenzionalne strukture GH92 v kompleksu z inhibitorji omogočajo vpogled v specifičnost, mehanizem in konformacijsko pot katalize.Ca(2+) igra ključno katalitično vlogo pri izkrivljanju manozida stran od konformacije osnovnega (4)C(1) stola proti prehodnemu stanju. (Bibliografija: Nat.Chem.Biol.6, 125-32, (2010)
Frontalna afinitetna kromatografija glikoasparaginov ovalbumina na koloni konkanavalina A-sefaroze.Kvantitativna študija vezavne specifičnosti lektina.
Interakcije konkanavalina A (ConA), imobiliziranega s Sepharose 4B, z 10 glikoasparagini, pridobljenimi iz ovalbumina, so kvantitativno raziskali s frontalno afinitetno kromatografijo.Pri tej metodi se raztopina ogljikovih hidratov neprekinjeno nanaša na kolono ConA-Sepharose, zaostanek elucijske fronte pa se meri kot parameter moči interakcije.Za vsak saharid s ConA je mogoče določiti disociacijsko konstanto (Kd).Analiza vezave p-nitrofenil-alfa,D-manozida je pokazala, da se vezavne lastnosti ConA po imobilizaciji na Sepharose 4B bistveno ne spremenijo.Vsak od glikoasparaginov ovalbumina je bil za analizo označen s tritijem z metodo reduktivne metilacije.Primerjava dobljenih vrednosti Kd je pokazala, da se vezava ConA precej spreminja z zelo majhnimi strukturnimi razlikami glikozilne verige.Rezultati kažejo, da ConA prepozna specifično strukturo glikozilne verige, Man alfa 1-6(Man alfa 1-3)Man, v kateri mora biti vsaj ena hidroksilna skupina na položaju C-3 C-6-povezane manoze prosta.