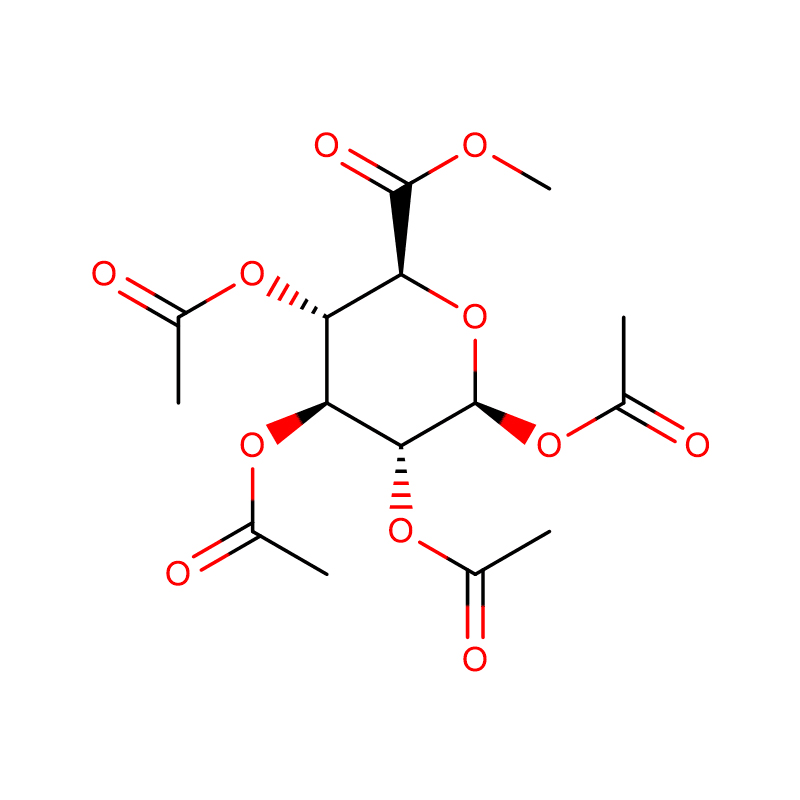
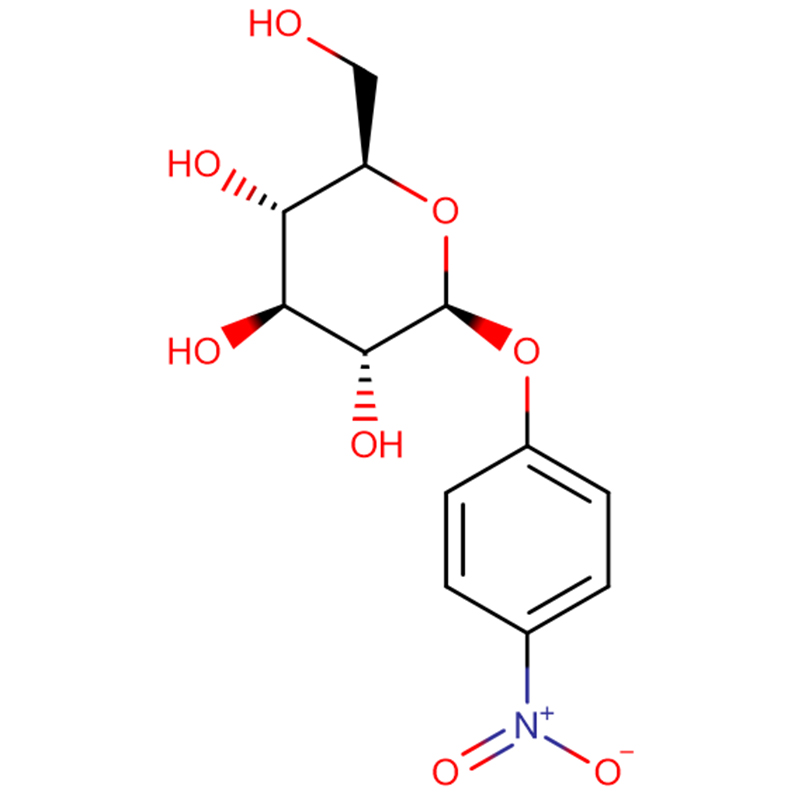
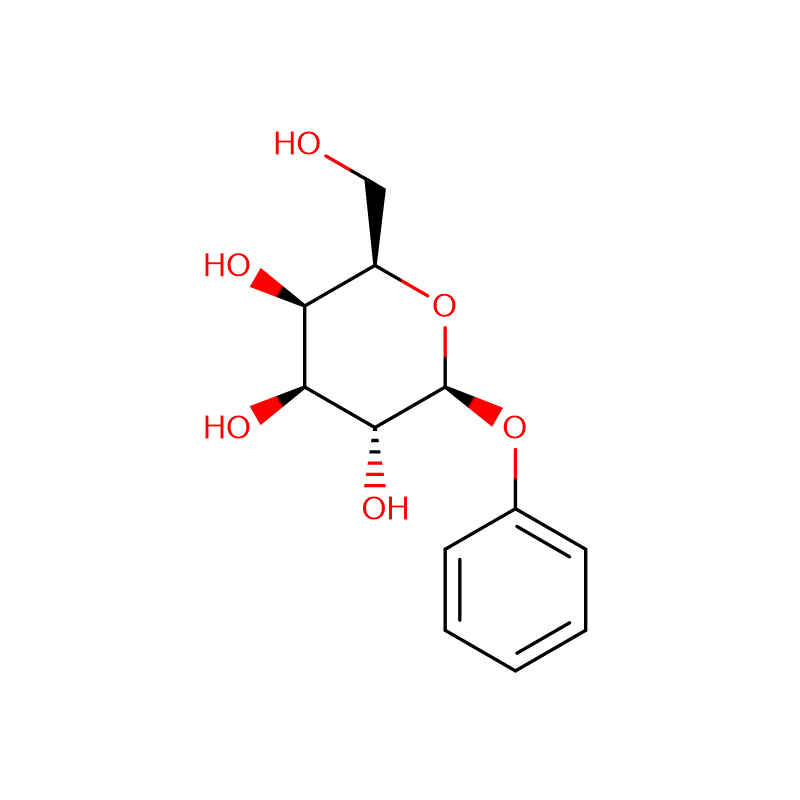
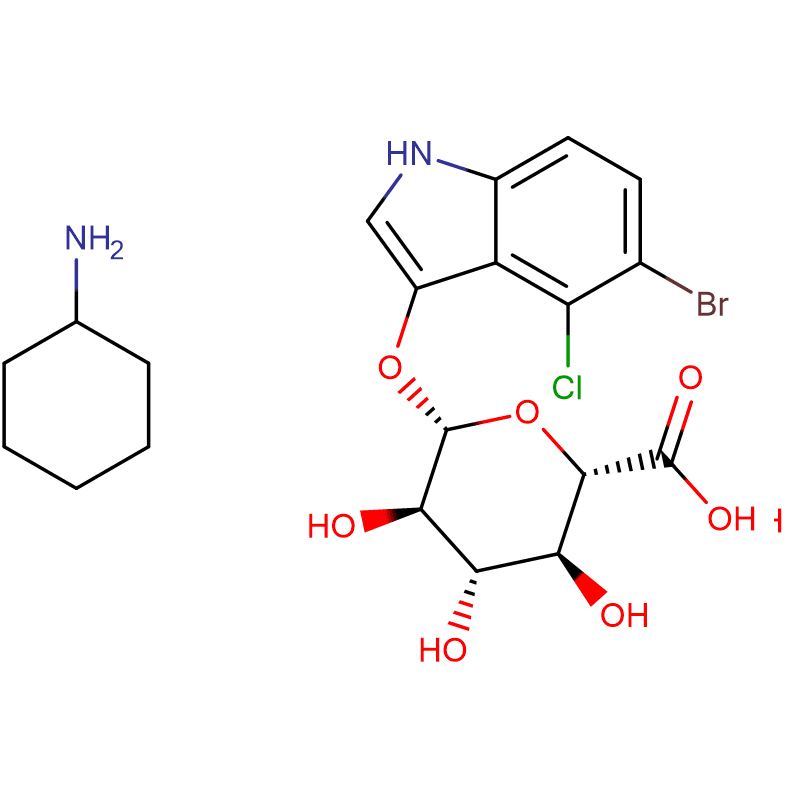
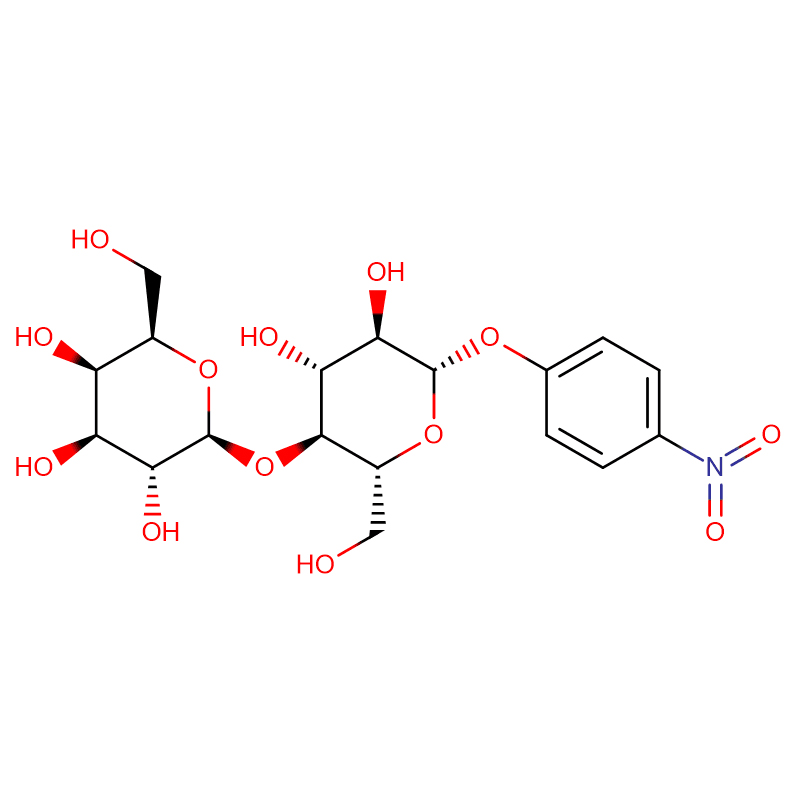
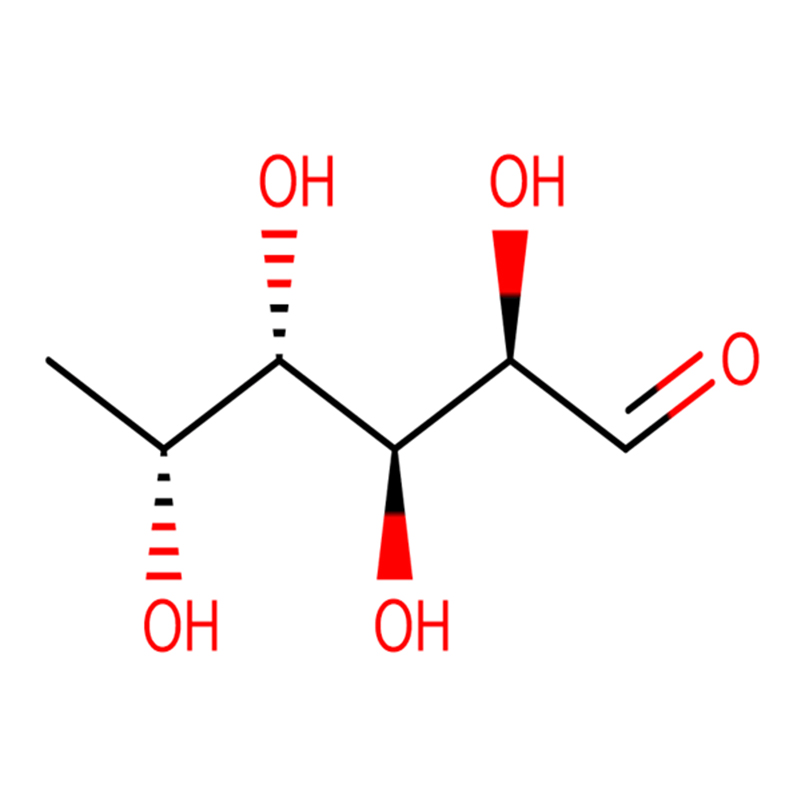
Dva izomerna biciklo[4.1.0]heptanska analoga inhibitorja glikozidaze galakto-validamina, (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(hidroksimetil)biciklo[4.1.0]heptana -2,3,4-triol, so sintetizirali v 13 korakih iz 2,3,4,6-tetra-O-benzil-D-galaktoze.Inhibitorne aktivnosti dveh konformacijsko omejenih aminov in njunih ustreznih acetamidov so merili proti komercialnim encimom alfa-galaktozidazo iz kavnega zrna in E. coli.Aktivnost encima GH27 iz družine glikozil hidrolaz (kavno zrno) je kompetitivno zaviral 1R,6S-amin (7), vezavna interakcija, za katero je bila značilna vrednost K(i) 0,541 mikroM.GH36 E. coli alfa-galaktozidaza je pokazala precej šibkejšo vezavno interakcijo z 1R,6S-aminom (IC(50)= 80 mikroM).Diastereomerni 1S,6R-amin (9) se je šibko vezal na obe galaktozidazi, (kavno zrno, IC(50)= 286 mikroM) in (E. coli, IC(50)= 2,46 mM).