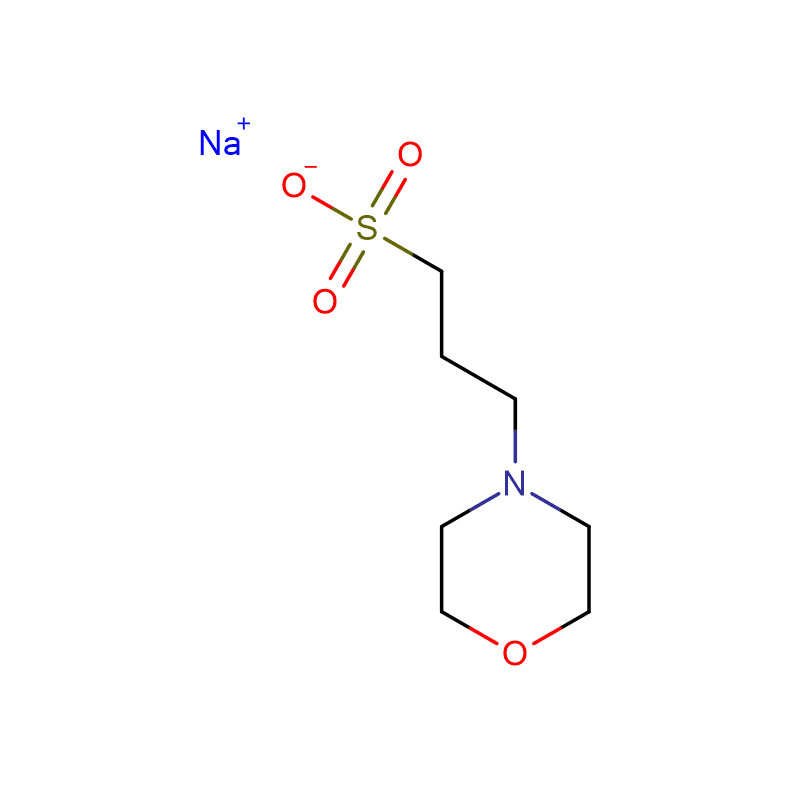
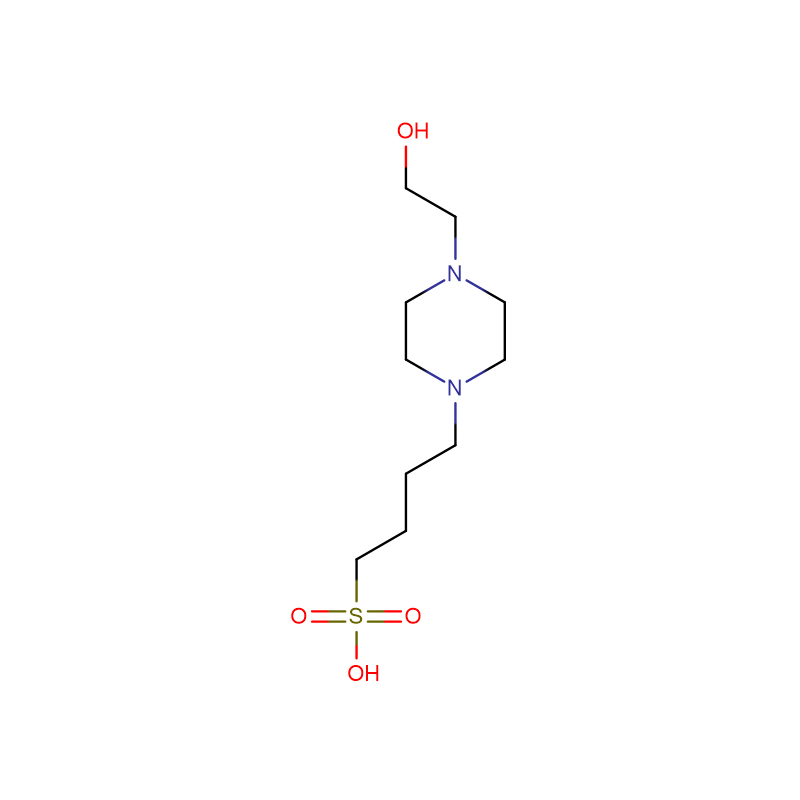
HEPBS Cas:161308-36-7 N-(2-hidroksietil)piperazin-N'-(4-butansulfonska kislina) bel kristaliničen prah 99%
| Kataloška številka | XD90100 |
| ime izdelka | HEPBS |
| CAS | 161308-36-7 |
| Molekularna formula | C10H22N2O4S |
| Molekularna teža | 266,36 |
| Podrobnosti o shranjevanju | Ambient |
| Usklajena tarifna oznaka | 2933599090 |
Specifikacije produkta
| Videz | Bel kristalinični prah |
| Assay | ≥ 99 % |
| Temp. shranjevanja | Shranjujte na RT |
| Tališče | 211-216 °C |
| Koeficient kislosti (pKa) | 8,3 (pri 25 ℃) |
Zavedamo se pomena zaščite celovitosti vaših biomolekul in reagentov s pravimi pufrskimi sistemi.Naši biološki pufri zagotavljajo stabilnost raztopine in nadzor pH brez motenj v bioloških procesih ter zagotavljajo kritične soli in hranila za celice in tkiva.Naši napredni puferski sistemi vam lahko prinesejo fenomenalno stabilnost pri celični kulturi, verižni reakciji s polimerazo (PCR), pregledovanju zdravil, bioprocesiranju, čiščenju in aplikacijah končne formulacije.Vse naše izdelke je mogoče razširiti od zgodnjih raziskav do komercialnih aplikacij v različnih stopnjah varovanja.Ponujamo številne konfiguracije pakiranja, mešanje po meri in celo tekoče formulacije.
Dobavljamo tudi obsežen izbor visokokakovostnih biokemikalij v praktičnih razredih in v različnih inovativnih, uporabniku prijaznih možnostih pakiranja.Poleg izdelkov, ki so že na prodajnih policah, nudimo izdelavo reagenta po meri, mešanje in pakiranje, ki ustreza vašim potrebam.
Načelo delovanja in vrednost pH puferske raztopine Ko nekaterim raztopinam dodamo določeno količino kisline in alkalij, ima učinek zaviranja spremembe pH raztopine, kar se imenuje puferski učinek.Takšna raztopina se imenuje puferska raztopina.Mešane raztopine šibkih kislin in njihovih soli (kot sta HAc in NaAc) ter mešane raztopine šibkih baz in njihovih soli (kot sta NH3·H2O in NH4Cl) so puferske raztopine.Puferski učinek pufrske raztopine, sestavljene iz šibke kisline HA in njene soli NaA, na kislino je posledica prisotnosti zadostne količine alkalije A- v raztopini.Ko tej raztopini dodamo določeno količino močne kisline, H ione v bistvu porabijo A- ioni: tako se pH raztopine skoraj ne spremeni;ko dodamo določeno količino močne baze, šibka kislina HA, prisotna v raztopini, porabi OH- ione, ki ovirajo spremembo pH.



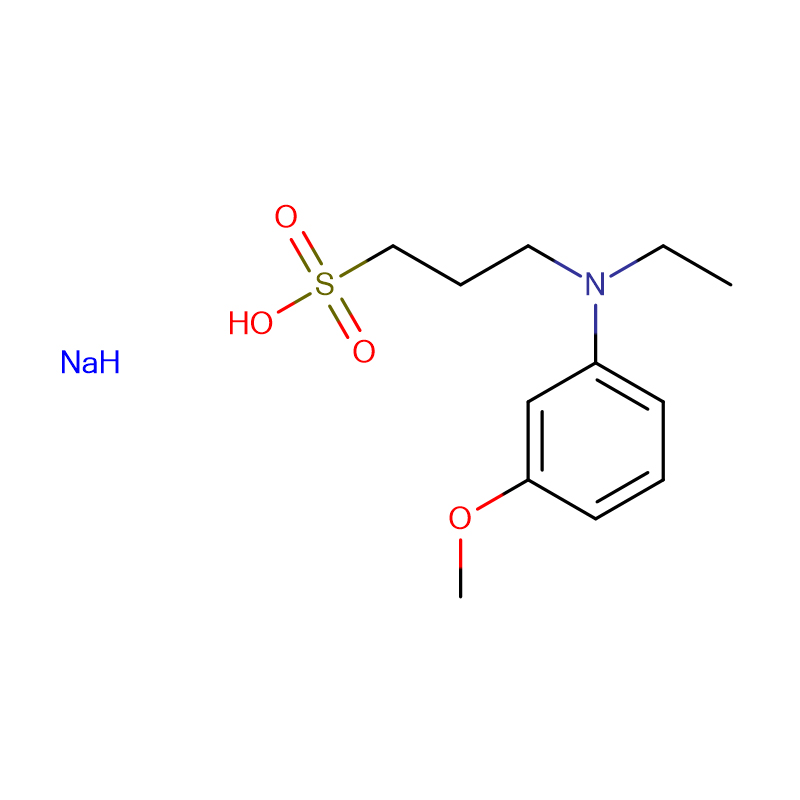
![TAPS-NA Cas:91000-53-2 tekoča 99 % natrijeva sol N-[tris(hidroksimetil)metil]-3-aminopropansulfonske kisline](http://cdn.globalso.com/xdbiochems/91000-53-2.jpg)